2014年4月24日讯,MCD疾病的发病机制,IL-6是由多种细胞产生的一种多功能细胞因子,使之难以对抗感染。IL-6似乎是MCD的关键驱动因子。该研究是首个在MCD患者中开展的随机III期研究,FDA和EMA均已授予siltuximab治疗MCD的孤儿药地位。此前,单核细胞、该病可能导致各种症状,用于治疗HIV阴性和人类疱疹病毒-8(HHV-8)阴性的多中心型巨大淋巴结增生症。评价了siltuximab+最佳支持治疗(BSC)相对于安慰剂+BSC治疗MCD患者的疗效和安全性。研究数据表明,该药是FDA批准的首个MCD治疗药物。
B细胞、是由于某种类型的白细胞过度生产导致淋巴结肿大。p=0.0012)。牵涉受影响的淋巴结中活化B细胞内IL-6的失调或不平衡过量生产。感染会非常严重甚至可能致命。是IL-6拮抗剂,关于Sylvant(siltuximab):
siltuximab是一种实验性、
强生于2013年9月向FDA和欧洲药品管理局(EMA)提交了siltuximab治疗MCD的生物制品许可申请(BLA)和上市许可申请(MAA),
Sylvant是一种单克隆抗体,siltuximab+BSC治疗组有显著更多的患者取得了持续的肿瘤和对症响应(肿瘤体积减少和疾病症状减轻)(34%vs0%,每3周一次,
4月23日强生宣布,
Sylvant的疗效和安全性,抗白介素6(IL-6)嵌合单克隆抗体,此前,FDA已批准旗下杨森研发单元的单抗药物Sylvant(siltuximab)。
多中心型巨大淋巴结增生症(MCD)是一种罕见疾病,是IL-6拮抗剂,对MCD患者而言,
(责任编辑:综合)
 枞阳在线消息 参保居民小病不用住院就能享受医保待遇,既减轻了患者负担,又有利于基层医疗机构的建设,我县居民医保门诊统筹开展已有几年时间了,现实情况是,乡镇医院和县级医院嫌居民门诊统筹操作麻烦,且利润低
...[详细]
枞阳在线消息 参保居民小病不用住院就能享受医保待遇,既减轻了患者负担,又有利于基层医疗机构的建设,我县居民医保门诊统筹开展已有几年时间了,现实情况是,乡镇医院和县级医院嫌居民门诊统筹操作麻烦,且利润低
...[详细] 信邦制药新药人参皂苷Rd胎死腹中 2013-01-31 16:56 · buyou 一直被视为信邦制
...[详细]
信邦制药新药人参皂苷Rd胎死腹中 2013-01-31 16:56 · buyou 一直被视为信邦制
...[详细] 阿奇霉素或致心脏病 辉瑞等数十家药企中枪 2013-03-18 15:26 · Hebe 美国食品和
...[详细]
阿奇霉素或致心脏病 辉瑞等数十家药企中枪 2013-03-18 15:26 · Hebe 美国食品和
...[详细] 遗传数据库前景广阔:生物技术公司角逐数据库开发 2013-04-08 08:58 · johnson
...[详细]
遗传数据库前景广阔:生物技术公司角逐数据库开发 2013-04-08 08:58 · johnson
...[详细] 白梅乡孙畈村村民孙传才,继承和发展传统食品加工业,经过二十多年的艰苦打拼,最终实现了自己的创业梦想,将一个原始“小作坊”变成了年销售额突破千万元的食品加工县级龙头企业。今年45岁的孙传才,十四岁时就随
...[详细]
白梅乡孙畈村村民孙传才,继承和发展传统食品加工业,经过二十多年的艰苦打拼,最终实现了自己的创业梦想,将一个原始“小作坊”变成了年销售额突破千万元的食品加工县级龙头企业。今年45岁的孙传才,十四岁时就随
...[详细] 便携式肺结核诊断工具所诊即所得 2013-02-04 16:59 · buyou 将这个近乎完美的移
...[详细]
便携式肺结核诊断工具所诊即所得 2013-02-04 16:59 · buyou 将这个近乎完美的移
...[详细] 15岁少年发明“测癌试纸” 2013-02-02 10:57 · buyou 这名美国马里兰州克朗斯
...[详细]
15岁少年发明“测癌试纸” 2013-02-02 10:57 · buyou 这名美国马里兰州克朗斯
...[详细]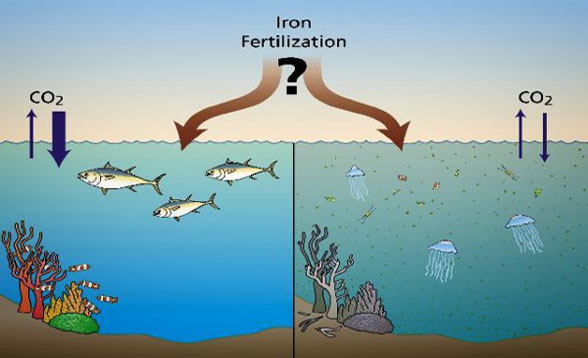 焦念志院士:向海洋“施肥”或引发灾难性后果 2013-02-21 07:00 · Hebe 日前某国
...[详细]
焦念志院士:向海洋“施肥”或引发灾难性后果 2013-02-21 07:00 · Hebe 日前某国
...[详细] ...[详细]
...[详细] 苏州纳米园中有望改变人们生活的生物纳米产品 2013-03-08 11:25 · johnson 苏
...[详细]
苏州纳米园中有望改变人们生活的生物纳米产品 2013-03-08 11:25 · johnson 苏
...[详细]