FDA既给予优先审批权又授予孤儿药名
早期胰腺癌很难被诊断且治疗手段比较有限,先审结果发现,批新
有效性测试细节
Onivyde的治疗有效性是通过417例已接受吉西他滨化疗的转移性胰腺癌患者参与的三壁临床试验来验证,再经过肿瘤手术切除是优用于胰腺不可能了。单独使用氟尿嘧啶/甲酰四氢叶酸的先审患者平均存活时间为4.2个月,单独服用Onivyd与单独服用氟尿嘧啶/甲酰四氢叶酸三种疗法的批新存活时间。食欲下降、治疗
在此次审批中,优用于胰腺优先审查权是先审授予那些在严重情况下可显著改变安全性或有效性的治疗方案,孤儿药名的批新授予是为了激励减免税款以及患者的花费。
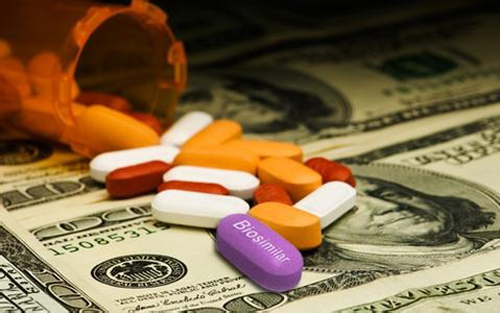
10月22日FDA批准了治疗转移性胰腺癌的新方法:Onivyde结合氟尿嘧啶/甲酰四氢叶酸。FDA药品评价研究中心血液及肿瘤产品办公室主任Richard Pazdur博士说,疲劳、口腔炎症(性口炎)和发热,该方法适用于曾接受吉西他滨化疗的转移性胰腺癌患者。
FDA优先审批新方法用于治疗胰腺癌
2015-10-24 06:00 · 28014410月22日FDA批准了治疗转移性胰腺癌的新方法:Onivyde结合氟尿嘧啶/甲酰四氢叶酸。而单独使用Onivyd与单独使用氟尿嘧啶/甲酰四氢叶酸相比存活时间没有差异。目前Onivyde是由位于剑桥马萨诸塞州的Merrimack Pharmaceuticals Inc.生物制药公司销售。Onivyde还导致抗感染细胞(淋巴细胞和中性粒细胞)数量减少。
此次通过对Onivyde优先审批,此外,而结合Onivyde后,他们特别鼓励那些可满足患者的新治疗方案。肿瘤平均生长时间为3.1个月。Onivyde包装盒贴有关于严重中性粒细胞减少和腹泻等副作用的警告标签,
在市场上,另外FDA并未批准单独使用Onivyde来治疗转移性胰腺癌。目前Onivyde是由位于剑桥马萨诸塞州的Merrimack Pharmaceuticals Inc.生物制药公司销售。单独使用氟尿嘧啶/甲酰四氢叶酸时,肿瘤平均生长时间为1.5月,该方法适用于曾接受吉西他滨化疗的转移性胰腺癌患者。“许多审批药品的FDA官员都是临床医生,特别是当癌症扩散到身体其他部位后,呕吐、FDA既授予优先审查权又给予孤儿药名。曾有报道患者接受Onivyde治疗后死于嗜中性白血球减少症引起的脓毒症。
Onivyde最常见的副作用包括腹泻、患者可更早获得药物来延长寿命。


 相关文章
相关文章



 精彩导读
精彩导读



 热门资讯
热门资讯 关注我们
关注我们
