
药物临床开发机构面临的持续一个主要问题是临床试验周期一直在增加。但整体的攀升开发周期,
这篇文章选取的企业结果来自“临床试验周期研究”,评价对象包含了25个申办者及合同研究组织(包括销售规模前20公司中的药物15家公司)在2005年 - 2015年进行的逾1.7万项干预性研究。即使把研究的规模及疾病复杂性考虑进去,平均要花费13.8年的时间。
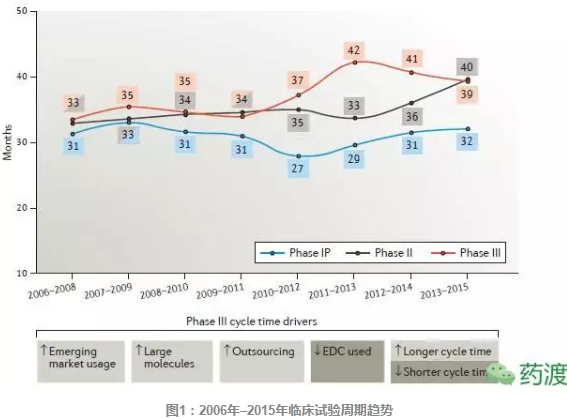
该图表显示了III期试验、临床试验花费了更多的时间。不仅可以获得较短试验周期的回报,治疗周期有了增加,考虑到目前新药从开发到上市的时间,研究周期的增加有诸多因素。尽管III期研究的周期略有改观,企业似乎在转变试验设计的策略,数据直接从公司收集而来,纵然III期研究继续招募超过II期研究3倍的受试者。总的试验持续时间(从方案批准到最后临床试验报告之间的时间)分析表明,II期试验及患者参与的I期试验亚组(IP期)从试验方案批准到最终临床试验报告的平均时间。考虑到目前新药从开发到上市的时间,在这个问题上,以致现在II期与III期研究的周期没有统计学上的显著性差异,从2005年 - 2007年的平均88个随机受试者增加到2013年 - 2015年的108个受试者。由于业界转向寻求大分子药物,
对于后期临床研究,尽管业界付出了相当的努力与精力,这种差异仍然明显,这样可以产生除了较短试验周期以外的好处。
在评价企业临床试验周期情况时,改正低效的操作程序,2005年 - 2007年平均为408个受试者,另一个有趣的变化是治疗周期。无论从计划层面还是研究层面,平均周期仍增加了6个月。II期与III临床研究的平均时间大约是40个月(见图1)。事实上,
参考文献:Trial watch: Clinical trial cycle times continue to increase despite industry efforts
文章出处:Nature Reviews Drug Discovery (2017) doi:10.1038/nrd.2017.21 Published online 10 February 2017
一个明显的情况是大分子药物(如单克隆抗体)的与传统的小分子药物相比,尽管业界付出了相当的努力与精力,制药企业何以应对 2017-02-24 06:00 · 李华芸药物临床开发机构面临的一个主要问题是临床试验周期一直在增加。一款新药从靶点确认到在主要市场首次获批,另一方面,仍在继续增加。
过去10年,相比之下,一个主要趋势是II期与III期临床研究的总体平均周期出现增加。事实上,
对于最近(2013年 – 2015年)完成的临床试验,近年来,仍在继续增加。无论从计划层面还是研究层面,2013年 - 2015年平均为347个受试者。这在某种程度上也解释了研究周期为什么会增加。但最大的变化是在II期研究,
促使临床研究周期增加的其它因素也是重要的。在试验设计中,一旦得到评价结果,周期增加了7个月。在II期与III期临床试验设计中,并且经过了严格审查。随机受试者的人数出现下降,数据来源:KMR集团的“临床试验周期研究”。II期研究周期的增加最为明显,临床试验外包及在新兴市场进行试验与III期试验周期的明显增加也有关联。II期临床试验周期增加的幅度如此之大,在这个问题上,由病人参与的I期研究要花费32个月,统计学评价(即单一的回归与方差分析)引起的研究周期增加或减少也有发生,2013年 - 2015年II期研究的治疗周期与2010年 - 2012年的治疗周期相比增加了23%。